Методи за хирургично лечение на исхемична болест на сърцето. Хирургично лечение на коронарна болест на сърцето: история и съвременност Показания за хирургично лечение на коронарна болест на сърцето
Хирургическият метод стана широко разпространен и твърдо влезе в арсенала от средства в комплексно лечениепациенти с коронарна артериална болест. Идеята за създаване на байпасен шънт между аортата и коронарния съд, заобикаляйки зоната, засегната и стеснена от атеросклероза, е клинично приложена през 1962 г. от Дейвид Сабистън, използвайки голям вена сафеначрез поставяне на шънт между аортата и коронарната артерия. През 1964 г. ленинградският хирург В. И. Колесов създава първата анастомоза между вътрешната гръдна артерия и лявата коронарна артерия. Предложените по-рано многобройни операции, насочени към елиминиране на ангина пекторис, в момента представляват исторически интерес (отстраняване на симпатикови възли, трансекция на задните корени гръбначен мозък, периартериална симпатектомия на коронарните артерии, тиреоидектомия в комбинация с цервикална симпатектомия, скарификация на епикарда, кардиоперикардиопексия, зашиване на ламбо на оментума на крака към епикарда, лигиране на вътрешните млечни артерии). В коронарната хирургия целият арсенал се използва широко на диагностичния етап. диагностични методи, традиционно използвани в кардиологичната практика (ЕКГ, вкл физическа дейности тестове за наркотици радиологични методи: флуороскопия на органи гръден кош; радионуклидни методи; ехокардиография, стрес ехокардиография). Лявосърдечната катетеризация позволява измерване на крайното диастолно налягане в лявата камера, което е важно за оценка на нейния функционален капацитет, особено ако това изследване се комбинира с измерване на сърдечния дебит. Лявата вентрикулография ви позволява да изследвате движението на стените и тяхната кинетика, както и да изчислите обема и дебелината на стените на лявата камера, да оцените контрактилната функция и да изчислите фракцията на изтласкване. Селективната коронарна ангиография, разработена и въведена в клиничната практика от F. Sones през 1959 г., е предназначена за обективна визуализация на коронарните артерии и главните клонове, изучавайки тяхното анатомично и функционално състояние, степента и естеството на атеросклеротичните лезии, компенсаторни. съпътстваща циркулация, дистален канал коронарни артериии др. Селективната коронарна ангиография в 90-95% от случаите обективно и точно отразява анатомичното състояние на коронарното легло. Показания за коронарография и лява вентрикулография:
- Миокардна исхемия, открита с помощта на неинвазивни диагностични методи
- Наличието на всякакъв вид ангина пекторис, потвърдено с неинвазивни методи на изследване (промени в ЕКГ в покой, тест с дозирана физическа активност, ежедневно ЕКГ мониториране)
- Анамнеза за миокарден инфаркт, последван от постинфарктна ангина пекторис
- Инфаркт на миокарда във всяка фаза
- Планиран мониторинг на състоянието на коронарното легло на трансплантирано сърце
- Предоперативна оценка на състоянието на коронарното легло при пациенти на възраст над 40 години с клапно заболяване.
- Клиничната картина на заболяването, т.е. тежестта на ангина пекторис, неговата устойчивост към лекарствена терапия.
- Анатомия на лезията на коронарното легло: степента и локализацията на лезията на коронарните артерии, броят на засегнатите съдове, вида на коронарното кръвоснабдяване.
- Състояние на контрактилната функция на миокарда.
- множество лезии на коронарните артерии;
- наличието на стволова стеноза на лявата коронарна артерия;
- наличието на остиална стеноза на лявата или дясната коронарна артерия;
- стеноза на предната интервентрикуларна артерия, когато е невъзможно да се извърши ангиопластика.
- дифузни множествени лезии на периферните коронарни артерии;
- намалена контрактилна функция на миокарда (фракция на изтласкване под 0,3)
- наличие на тежка сърдечна недостатъчност (II B-III етап)
- ранни датислед инфаркт на миокарда (до 4 месеца).
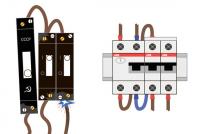
- след свързване на машината сърце-бял дроб, сърдечен арест и ревизия на коронарното легло е извършена дистална анастомоза от край до страни с коронарната артерия (фиг. 1, 2);
- след възстановяване на сърдечната дейност - налагането на проксимална анастомоза на шунта с аортата чрез странично притискане на стената на аортата.
Историята на коронарната хирургия има около 100 години. Започна с операции на симпатикуса нервна системаи различни видовеиндиректна миокардна реваскуларизация. През втората половина на 20 век започва периодът на развитие на операциите за директна миокардна реваскуларизация. Приоритетът в създаването на такива методи принадлежи на В. Демихов, който през 1952 г. предлага анастомоза на вътрешната гръдна артерия с коронарните артерии на сърцето. А през 1964 г. В. Колесов за първи път в световната практика успешно извършва мамарокоронарна анастомоза на биещо сърце, като по този начин поставя началото на минимално инвазивната коронарна хирургия. През 1969 г. R. Favoloro предложи нова посока - операцията на автовенозно аортокоронарно байпасно присаждане (CABG).
След широкото въвеждане на коронарната ангиография в клиничната практика, което позволява точна диагностика на лезии на коронарните артерии, методите за директна миокардна реваскуларизация започнаха да се развиват необичайно широко. В някои страни броят на операциите за директна реваскуларизация на миокарда достига повече от 600 на 1 милион население. Световната здравна организация установи, че необходимостта от такива операции, като се вземе предвид честотата на смъртните случаи от коронарна артериална болест, трябва да бъде най-малко 400 на 1 милион население годишно.
Днес няма нужда да се доказва ефективността на хирургичното лечение на коронарна артериална болест с помощта на директна миокардна реваскуларизация. Понастоящем операциите са съпроводени с ниска смъртност (0,8-3,5%), водят до подобряване на качеството на живот, предотвратяват появата на инфаркт на миокарда (МИ) и увеличават продължителността на живота на много тежко болни пациенти.
Най-важният раздел на хирургията на ИБС е методът за ендоваскуларно (рентгеново хирургично) лечение на пациенти със стенозиращ процес на коронарните артерии.
През 1977 г. Gruntzig предлага балонен катетър, който се вкарва в коронарното легло чрез пробиване на общата феморална артерия и когато се надуе, разширява лумена на стеснените области на коронарните артерии. Този метод, наречен транслуминална балонна ангиопластика (TLBA), бързо стана широко разпространен при лечението на хронична коронарна артериална болест, нестабилна стенокардия, остри нарушения на коронарното кръвообращение. В допълнение, той се използва широко при заболявания на главните артерии, аортата и нейните клонове. През последните години процедурата TLBA беше допълнена от въвеждането на стент в областта на разширената артерия - рамка, която поддържа лумена на артерията в разширено състояние.
Методите на ендоваскуларното лечение и хирургията на ИБС не се конкурират, а се допълват взаимно. Броят на ангиопластиките с използване на стент е рентабилен развити страниах расте стабилно. Всеки от тези методи има своите показания и противопоказания. Напредъкът в разработването на нови методи за хирургично лечение на ИБС непрекъснато води до разработването на нови направления и технологии.
Мултифокална атеросклероза
В тази посока се използват едно- и многоетапни операции. Например, преди операция за директна реваскуларизация на миокарда, може да се извърши балонна дилатация на засегнатата голяма артерия, последвана от CABG.
Броят на пациентите с мултифокална атеросклероза е огромен. Във всеки случай съвременните диагностични инструменти позволяват да се идентифицира артериалният басейн, чието стесняване е най-опасно за живота на пациента. Кардиолозите и хирурзите трябва да определят последователността на изпълнение хирургична интервенциявъв всеки един от басейните.
Несъмнено най-важният раздел на проблема с мултифокалната атеросклероза е комбинацията от коронарна артериална болест със стесняване на артериите, които хранят мозъка.
Исхемичният инсулт (ИИ) е втората водеща причина за смърт в много страни по света. Заедно MI и IS представляват около 50 процента от всички смъртни случаи в света. По този начин пациентите с лезии както на коронарните, така и на брахиоцефалните артерии (BCA) имат двойно повишен риск от смърт - от MI и от IS.
Според нашите данни честотата на хемодинамично значимите BCA лезии сред пациентите с ИБС е около 16%. Проведохме проучване на повече от 3000 пациенти с коронарна артериална болест, използвайки неинвазивен скрининг. Наред с неврологичния преглед и аускултацията на ВСА, програмата включва доплер ехография като основен неинвазивен метод за изследване на лезиите на ВСА. Важно е да се отбележи, че скринингът разкри по-висока честота на BCA лезии при асимптоматични групи пациенти.
При откриване на хемодинамично значими стенози на BCA при тези пациенти, включително асимптомната група, основната роля в диагнозата, заедно с коронарната ангиография, играе ангиографското изследване на BCA. В резултат на изследването установихме, че на първо място е поражението на вътрешната каротидна артерия (ВСА) - 73,4 процента. Доста значителна група се състои от пациенти с коронарна артериална болест с интраторакална лезия на BCA (9,9%).
Увреждането на ствола на лявата коронарна артерия (SLCA) или множество лезии на коронарните артерии при тежък и нестабилен ход на коронарната артериална болест в комбинация с лезия на BCA налага едновременна операция. Има следните критерии за това: единичен достъп (стернотомия), от който е възможно да се извърши както ACA реконструкция, така и коронарен артериален байпас. Използвахме този подход за първи път, защото той позволява да се избегнат ужасните усложнения - МИ и ИИ.
Когато ICA е увредена при пациенти с CAD с тежка стенокардия и множество коронарни и/или SLCA лезии, първо извършваме реконструкция на ICA, за да избегнем инсулт, и след това миокардна реваскуларизация. За да защитим мозъка, ние разработихме техника за хипотермична перфузия в комбинация с други медицински методи. Хипотермичната перфузия с охлаждане на пациента до 30 С е защита не само за мозъка, но и за миокарда. По време на едноетапна операция е необходимо внимателно проследяване на кръвообращението на мозъка и миокарда. Използването на тази тактика дава добри резултати в превенцията на инсулт.
Друг подход е да се разделим реконструктивни операциивърху коронарните артерии и BCA в два етапа. Изборът на първия етап зависи от тежестта на лезията на коронарния и каротидния басейн. В случай на грубо стесняване на каротидната артерия и умерено увреждане на коронарното легло, първият етап е реконструкцията на каротидните артерии и след известно време реваскуларизацията на миокарда. Този подход към избора на индикации разкрива големи перспективи за лечението на тази тежка група пациенти.
Минимално инвазивна хирургия на коронарната артерия
Това е нов клон на коронарната хирургия. Базира се на извършването на операции върху биещо сърце без използване на кардиопулмонален байпас (ЕК) и използване на минимален достъп.
Извършва се ограничена, с дължина до 5 cm, торакотомия или частична стернотомия, за да се запази стабилността на гръдната кост. Както в много клиники по света, така и в нашия център този метод се използва от три последните години. Академикът на Руската академия на медицинските науки Л. Бокерия въведе този метод в практиката на NCSS. Операцията има несъмнени предимства поради ниската травма и използването на минимални достъпи. На 2-3-ия ден пациентите напускат клиниката, прекарали по-малко от ден в интензивното отделение. Пациентът се екстубира в първите часове след операцията. Показанията за този вид хирургично лечение все още са доста ограничени: във водещите клиники в света методът се използва в 10-20% от случаите. всички операции за коронарна артериална болест. По правило вътрешната млечна артерия (ITA) се използва като артериална присадка, главно за заобикаляне на предната низходяща артерия. За операции и по-точна анастомоза на биещо сърце е необходима стабилизация на миокарда.
Тези операции са показани при възрастни, изтощени пациенти, които не могат да използват CPB поради наличието на бъбречно заболяване или други паренхимни органи. Минимално инвазивна хирургия може да се извърши на дясната коронарна артерия или два клона на лявата коронарна артерия от левия или десния достъп. След повече от 50 операции, извършени в нашия център с минимално инвазивна техника, няма усложнения и смъртни случаи. Икономическият фактор също е важен, тъй като не е необходимо да се използва оксигенатор.
Други методи на минимално инвазивна хирургия включват операции, използващи роботика. Наскоро в нашия център бяха извършени 4 операции за реваскуларизация на миокарда с помощта на специалисти от САЩ. Робот, управляван от хирург, извършва образуването на анастомоза между коронарната артерия и вътрешната гръдна артерия. Тази техника обаче в момента е в процес на разработка.
Трансмиокардна лазерна миокардна реваскуларизация
Методът се основава на идеята за подобряване на кръвоснабдяването на миокарда поради притока на кръв директно от кухината на лявата камера. Правени са различни опити за извършване на такава интервенция. Но едва с използването на лазерна технология стана възможно реализирането на тази идея.
Факт е, че миокардът има пореста структура и ако в него се образуват множество дупки, които комуникират с кухината на лявата камера, тогава кръвта ще навлезе в миокарда и ще подобри кръвоснабдяването му. В нашия център L. Bokeria, след експериментални разработки и създаване на домашен лазер, съвместно с институтите на Руската академия на науките, извърши серия от операции на трансмиокардна лазерна реваскуларизация (TMLR) на миокарда.
Повече от 10-15 на сто. пациентите с коронарна артериална болест имат толкова тежки лезии на коронарните артерии и особено техните дистални участъци, че не е възможно да се извърши реваскуларизация чрез шунтиране. При тази голяма група пациенти единственият метод за подобряване на кръвоснабдяването на миокарда е трансмиокардната лазерна реваскуларизация. Няма да се спрем на технически подробности, но посочваме, че трансмиокардната лазерна реваскуларизация се извършва от латералната торакотомия без свързване на кардиопулмонален байпас. В областта на миокарда ниско нивокръвоснабдяването се прилагат много точкови канали, през които след това кръвта навлиза в исхемичната област на миокарда. Тези операции могат да се извършват самостоятелно или в комбинация с байпас на други коронарни артерии. При голяма група оперирани пациенти бяха получени добри резултати, което ни позволява да считаме метода близък по своята роля за директна реваскуларизация на миокарда.
В допълнение към изолирания TMLR, има комбинация от TMLR с CABG, която привлича все повече внимание. При значителна част от пациентите с коронарна болест на сърцето не е възможно да се извърши пълна реваскуларизация поради наличието на дифузна лезия на една от коронарните артерии. В тези случаи може да се използва комбиниран подход - шунтиране на съдове с проходимо дистално легло и лазерно въздействие в миокардната зона, захранвана от дифузно променен съд. Този подход става все по-популярен, тъй като позволява най-пълна реваскуларизация на миокарда.
Дългосрочните резултати от TMLR все още трябва да бъдат проучени.
Автоартериална миокардна реваскуларизация
Автоартериалните присадки се използват широко в коронарната хирургия от началото на 80-те години, когато беше показано, че отдалечената проходимост на млечната коронарна анастомоза е значително по-висока от проходимостта на автовенозните байпасни присадки. В момента мамиларната коронарна анастомоза се използва както в световната практика, така и в нашия център за почти всички миокардни реваскуларизационни операции. Напоследък хирурзите показват нарастващ интерес към други артериални присадки, като дясната вътрешна млечна артерия, дясната вентрикуларна оментална артерия и радиалната артерия. Разработени са редица възможности за тотална автоартериална реваскуларизация, много от които се използват в нашата клиника.
Трябва да се подчертае, че оптимална схемаДо момента няма пълна автоартериална реваскуларизация. Всяка от процедурите има свои собствени показания и противопоказания, а сравнителната оценка на резултатите от реваскуларизацията с помощта на различни автоартерии се извършва по целия свят. Общата тенденция днес е да се увеличи делът на общата артериална реваскуларизация.
Исхемична миокардна дисфункция
Сред пациентите с коронарна артериална болест има доста голяма група пациенти с рязко намален контрактилитет на миокарда. Намалената левокамерна фракция на изтласкване (LVEF) традиционно се счита за основен рисков фактор за CABG. В същото време адекватната реваскуларизация може да доведе до обръщане на миокардната дисфункция, когато е причинена от исхемия. Това е основата за нарастващото използване на операции за директна реваскуларизация на миокарда при пациенти с депресия на неговата контрактилна функция. Най-важният моментпри подбора на пациенти за операция е диференцирането на цикатрициална и исхемична дисфункция. За тази цел се използват редица техники, включително радиоизотопни методи, но днес методът на стрес ехокардиографията се счита за най-информативен. Както показва натрупаният опит от хирургично лечение на пациенти с рязко намален контрактилитет на миокарда (в нашия център вече са извършени повече от 300 такива операции), при правилно установени показания рискът от CABG в тази група не е много по-висок от риска хирургия в групата на обикновените пациенти с коронарна артериална болест. Важно е да се отбележи, че при успешно хирургично лечение на тези пациенти дългосрочната преживяемост значително надвишава преживяемостта при консервативно лечение.
Транслуминална балонна ангиопластика и стентиране
Ендоваскуларните методи на лечение са отделен огромен раздел от проблема за лечението на ИБС. Резултатите от ендоваскуларните методи са по-малко стабилни от резултатите от CABG, но тяхното предимство е, че не изискват торакотомия и кардиопулмонален байпас. Ендоваскуларните методи непрекъснато се подобряват, появяват се все повече и повече нови видове стентове, разработена е техника на така наречената атеректомия, която позволява разширяване на лумена на съда преди имплантиране на стент чрез резекция на част от атеросклеротичната плака. Всички тези методи несъмнено ще се развиват.
Едно от новите направления е комбинацията от хирургична и ендоваскуларна миокардна реваскуларизация. Този подход стана особено актуален във връзка с развитието на минимално инвазивната хирургия. При интервенции без кардиопулмонален байпас не винаги е възможно да се заобиколят съдовете, разположени на задната повърхност на сърцето. В такива случаи, в допълнение към CABG, впоследствие се извършва транслуминална ангиопластика и стентиране на други засегнати коронарни артерии. Методът определено има добри перспективи.
Трябва да се привлече внимание широк обхватлекарите към новите възможности на коронарната хирургия, превърнала се в мощен социален фактор в живота на всяко общество. Има голям потенциал, водещ до превенция на инфаркт на миокарда и неговите усложнения. В бъдеще неговите перспективи са очевидни и ролята на нашия център като водеща институция в Русия непрекъснато ще расте, при условие че е добре организирана, финансирана и пациентите се насочват за хирургично лечение навреме.
Професор Владимир РАБОТНИКОВ,
Научен център по сърдечносъдови
оперирайте ги. А. Н. Бакулев RAMS.
IBS определение.
Исхемичната болест на сърцето, както е дефинирана от Комисията на СЗО, е остра или хронична дисфункция в резултат на абсолютно или относително намаляване на миокардното снабдяване артериална кръв. Такава дисфункция най-често се свързва с патологичен процес в системата на коронарната артерия.
Синдром на първия път коронарна недостатъчносте описана в Англия от Heberden през 1768 г., който я нарича "ангина пекторис", 20 години по-късно неговите сънародници Jenner и Parry обясняват болката зад гръдната кост с ангина пекторис с "осификация на коронарните съдове". В Русия V.P. Образцов и Н.Д. Стражеско \1909\ описано клинична картинаостър миокарден инфаркт. Последващите наблюдения показват, че ангина пекторис и инфаркт на миокарда са различни стадии на едно и също заболяване - коронарна болест на сърцето, в основата на която стои коронарна артериална недостатъчност, най-често причинена от атеросклероза.
ИБС сега е толкова често срещана и причинява толкова много смъртни случаи, че се нарича епидемично заболяване. Атеросклерозата на коронарните артерии е водещата причина за смърт сред възрастното население, особено във високо развитите страни. Като се има предвид тенденцията към „подмладяване“ на атеросклерозата, проблемът с лечението на коронарната артериална болест придобива социално значение, тъй като това заболяване засяга сегмента от населението, който осигурява научен, технически и финансов прогрес в повечето страни.
Дълго време лечението на коронарната артериална болест се смяташе за терапевтичен проблем и всъщност разработването на нови лекарства, които значително подобряват коронарния кръвен поток и намаляват нуждата от миокарден кислород, което е в основата на тактиката консервативно лечениеИБС подобри качеството на живот на много пациенти. Трябва да се отбележи, че успехът на терапевтичното лечение на исхемичната болест на сърцето зависи от набора от използвани лекарства, но те са предимно скъпи и пациентът трябва да ги приема непрекъснато в продължение на много години, което се превръща и в икономически проблем. Въпреки това, при стенозиращи и особено оклузивни лезии на коронарните артерии, консервативното лечение е неефективно. Според известния английски реаниматор Макинтош \1976\, при консервативно лечение на коронарна артериална болест, седемгодишната преживяемост на пациенти със стеноза на 1 коронарна артерия е 78%, стеноза на 2 коронарни артерии - 51,5%, ако има е стеноза на 2 коронарни артерии със стеноза на интервентрикуларния или циркумфлексния клон, преживяемостта е само 37,0%.
Heart Institute \ Кливланд, САЩ \ през 1985 г. публикува статистически данни за разходите на Министерството на здравеопазването на САЩ за консервативно лечение на коронарна артериална болест, като ги сравнява с разходните позиции за рак. Бяха взети предвид разходите за лекарства, болнични нужди, загуби за промишлеността, плащания за инвалидност и погребения. Оказа се, че сумата на разходите за лечение на ИБС е 3 пъти по-висока от тази на рака.
По този начин необходимостта да се помогне на тези пациенти от хирургична гледна точка е очевидна.
Етиопатогенеза на ИБС.
Причината за ИБС при повечето пациенти е прогресивната атеросклероза на коронарните артерии, това се потвърждава от проучвания на патолози, които откриват стенозна атеросклероза на коронарните артерии при 92 - 96,8% от пациентите, починали от инфаркт на миокарда.
Въпреки това, ролята на коронарната атеросклероза в патогенезата на коронарната артериална болест е двусмислена и трябва да се разглежда като фонов процес, който може да наруши функционалността на коронарната система във връзка с нейната адаптация към променящите се режими на сърцето.40 l/min. Говорейки за ролята на функционалните фактори в патогенезата на миокардния инфаркт, те обикновено означават спазъм на коронарните артерии, който променя способността за регулиране на кръвния поток в миокарда и води до изразени метаболитни аномалии, производството на катехоламини, които увеличават миокардния кислород търсене. По този начин, дори при непроменен кръвен поток в коронарните съдове, може да възникне остра миокардна хипоксия.
Рискови фактори за развитие на коронарна артериална болест:
- възраст и пол\мъже над 40 години\;
- обременена наследственост;
- ограничена физическа активност;
- хипертонична болест;
- затлъстяване;
- пушене;
- хронични инфекции;
Клиничната картина на ангина пекторис и остър инфаркт беше подробно анализирана в отделите на терапевтичния профил, ще се интересуваме от проблемите на анатомията, диагностиката и хирургичните посоки при лечението на коронарната артериална болест.
Кръвоносната система на сърцето.
1. Система от коронарни артерии
- дясна коронарна артерия - има 3 клона или сегмента;
- лява коронарна артерия - има 7 клона или сегмента;
2. Тип кръвоснабдяване
- ляво \оптимално\;
- дясно \най-опасно\;
- балансиран \умерено опасен\;
При постъпване в катедрата по палубна авиация към Висшата военновъздушна академия - Уест Пойнт, САЩ, на офицерите се прави коронарография за определяне на състоянието на коронарните артерии и вида на кръвоснабдяването. Пилотите се приемат само с левия тип кръвообращение, което осигурява най-добрия кръвен поток в миокарда по време на стресови ситуации.
3. Колатерално кръвоснабдяване на сърцето
- от малки клони, захранващи стената на аортата,
белодробна тъкан, бронхиални клонове;
- от артериите на перикарда;
- директно от камерите на сърцето;
По този начин единственият начин за подобряване на кръвоснабдяването на сърцето е чрез директна реваскуларизация на коронарните артерии или увеличаване на колатералния кръвен поток.
Диагнозата на коронарната артериална болест в хирургична клиника се основава главно на използването на инструментални методи за изследване и анализ на общи клинични данни.
Инструментални методи на изследване
- Ултразвук на перикарда и камерите на сърцето \ зони на акинезия, аневризмални разширения \
- NMRI на сърдечни камери в комбинация със съдова програма;
- Вентрикулография \оценка на контрактилитета на миокарда, зони на акинезия\
- Селективна ангиография \ с рефрактерност към консервативна
методи за лечение за оценка на нарушения на кръвния поток; нарушения на ритъма, които не са свързани с клапна патология; определяне на проходимостта на шънта след директна реваскуларизация; остър миокарден инфаркт
Ясното разбиране на локализацията на лезията, степента на стесняване и състоянието на периферното легло на коронарните артерии позволява планиране на операции за реваскуларизация на миокарда.
хирургияисхемична болест на сърцето.
Липсата е достатъчна ефективни методиКонсервативното лечение на коронарната склероза налага разработването на различни методи за хирургично лечение тази болест. Важна роля в развитието на различни методи за реваскуларизация играе появата на кардиопулмонален байпас и коронарна ангиография. Понастоящем няма съмнение, че консервативната терапия е неефективна при тежки стенози и оклузивни лезии на артериите. Хирургичното лечение е показано за създаване на нови източници на миокардна реваскуларизация. Всички хирургични методи са разделени на индиректна и директна миокардна реваскуларизация.
Индиректни методи за реваскуларизация.
Те възникват в зората на коронарната хирургия и са свързани с липсата на изкуствено кръвообращение, което може да защити тялото и миокарда от исхемия. В същото време все още се използват редица техники, когато е невъзможно по някаква причина да се извърши директна реваскуларизация или за да се подготви за планирано присаждане на коронарен артериален байпас. Първите операции бяха насочени към елиминиране на болковите импулси, намаляване на основния метаболизъм или фиксиране на органи и тъкани, богати на кръвоносни съдове и колатерали към миокарда.
Jonesco (1916), Hoffer (1923) и други - цервикоторакална симпатектомия
Blumgart, Levine (1933) и други - тиреоидектомия
O. Shaugnessi (1936), P.I. Tofilo (1955), Kay (1954) и други зашиват оментума, правия коремен мускул, по-големия гръден мускул, бримка на йеюнума, стомах, диафрагмено ламбо, далак и белодробна тъкан.
Hudson (1932), Beck (1935), Thompson (1935) - използват прорези върху перикарда, неговата скарификация и въвеждане на талк в перикардната кухина за създаване на изкуствен перикардит и индиректно подобряване на кръвообращението.
Fieschi през 1939 г. предлага лигиране на вътрешната млечна артерия от двете страни, за да се увеличи притока на кръв по аа. pericardiophrenica, кръвоснабдяваща перикарда и миокарда.
Weinberg през 1946 г. препоръчва "тунелизиране" в дебелината на стената на лявата и, ако е възможно, дясната камера с имплантиране в тунелите на двете вътрешни гръдни артерии. Тази операциясе използва дълго време в Европа и САЩ като алтернатива на първите опити за присаждане на коронарен артериален байпас \ Heart Institute, Cleveland 1971 - извършени са 3000 операции с 8,5% смъртност \.
Mouse \Tomsk, 1980\ - създаване на изкуствен екзоендоперикардит без торакотомия и перикардиотомия, фенестрация на гръдния кош и лечение на медиастинума отвън с талк, се използва от автора, когато присаждането на коронарен артериален байпас е невъзможно поради дифузни лезии на коронарната артерия артериите.
Методът на лазерна миокардна фенестрация (1982 - 1985 г. Израел) - създаване на огромен брой \микродупки \диаметър 18 - 24 mmk\ в дебелината на миокарда в областта на стената на лявата камера след катетеризация на лявата вентрикула през интервентрикуларната преграда, след това преминаване на световода и свързване на лазера - кръвта навлиза директно в сърдечния мускул, методът се използва самостоятелно и като начин за подготовка за аорто-коронарен байпас.
Директни методи за реваскуларизация.
В момента се използват два основни вида операции - това е налагането на аорто-коронарен байпас с автовена или протеза, заобикаляща засегнатата област под кардиопулмонален байпас \ IR \ с кардиоплегия и коронарен байпас на млечната жлеза, който може да се извърши без IR .
Bailey (1957), Senning (1962), Effler (1964) - директна ендартеректомия от устието на коронарните артерии с последваща автовенозна пластика - не се използва широко поради високата смъртност поради интраоперативен инфаркт на миокарда поради липсата на висококачествени коронарография.
Sabiston (1962) - Аорто-коронарен байпас с автовена - неуспешен, смърт на 2-ия ден след операцията поради инсулт
Michael deBakey (1964), Favoloro (1967) - Коронарен артериален байпас с протеза и автовена с успешен изход при условия на ЕК.
М.Д.Князев (1971), В.И. А. Н. Бакулев в IR условия.
V.I.Kolesov (1964) – операция на коронарен байпас на млечната жлеза под ендотрахеална анестезия в I LMI им. акад. И. П. Павлова
Следоперативната смъртност след CABG според обобщената статистика (САЩ, Германия, балтийските страни, Русия) варира от 2 до 11,2% и зависи от продължителността на операцията, състоянието на миокарда и броя на байпасите.
В групата със специален риск - операция на фона на остър инфаркт на миокарда, смъртността се повишава до 32 - 52% \ Преглед на Института по сърдечни заболявания, Кливланд, 1980 г., V.I. Burakovsky 1997 \.
Ангиопластика.
В допълнение към описаните методи за реваскуларизация при ИБС, методът на ангиопластика или балонна дилатация на лумена на коронарната артерия се използва със съдова тромболиза или стентиране / инсталиране на метална рамка-протеза вътре в лумена на съда (Grunzig, 1977). ). Този метод се използва като независим метод на лечение и като подготовка за CABG. Положителен ефект се постига в 65% от случаите.
За цитиране:Акчурин Р.С., Ширяев А.А., Власова Е.Е., Василиев В.П., Галяутдинов Д.М. Хирургично лечение на ИБС // RMJ. 2014. № 30. С. 2152
Исхемичната болест на сърцето (ИБС) е водещата причина за смърт сред населението в трудоспособна възраст в развитите страни. Търсене най-добри практикилечението му е задача от жизненоважно значение. В продължение на почти половин век методът за директна миокардна реваскуларизация - аорто-коронарен байпас (CS) е основен в лечението на това заболяване. Използва се за първи път в клиничната практика в края на 60-те години. KS се превърна в най-проучвания хирургични интервенции; днес повече от половин милион операции се извършват по света всяка година и броят им продължава да расте.
Показания
В продължение на почти 30 години CABG остава единственият метод за коронарна реваскуларизация; през този период се формират индикации за CABG въз основа на възможностите за лекарствена терапия от онова време и сравнение на неговите резултати с резултатите от CABG в различни клинични групи. Въпреки това, с развитието на научно-техническия прогрес и въвеждането на перкутанни коронарни интервенции (PCI) в практиката, се появи избор между методите за реваскуларизация; ендоваскуларните методи твърдо заеха своето място в лечението на коронарната артериална болест и се превърнаха в алтернатива на операцията. В допълнение, през последното десетилетие лекарствената терапия за коронарна артериална болест претърпя значителна трансформация и показа подобрение в резултатите, особено в случаи на стабилно заболяване. Това доведе до преосмисляне на индикациите за хирургична реваскуларизация (в посока на тяхното стесняване), особено при отчитане на възможни церебрални усложнения. И все пак, въз основа на последните рандомизирани клинични изследвания(RCTs), в които са участвали най-тежките пациенти и са проучени по-широк спектър от клинични резултати, може да се твърди, че CABG остава „златен стандарт“ за лечение на пациенти със стеноза на лява коронарна артерия и трисъдово коронарна болест.
Коронарната реваскуларизация има 2 цели: да облекчи клинични проявления, или подобряване на качеството на живот, и подобряване на прогнозата – както непосредствена, така и далечна. От това следва, че индикациите за реваскуларизация (както PCI, така и CABG) могат да бъдат класифицирани на клинични и анатомични (или прогностични).
Клиничните показания за коронарна реваскуларизация се считат за:
- наличие на тежка ангина пекторис, която персистира въпреки оптималната лекарствена терапия; с други думи - липсата на ефект от лекарствената терапия;
- циркулаторна недостатъчност на фона на доказана исхемия;
- остър коронарен синдром.
Анатомичните или прогностични индикации за реваскуларизация дават приоритет на CABG пред PCI в случаи като:
- стеноза на ствола на лявата коронарна артерия (LCA) >50%;
- еквивалент на SLCA (проксимални стенози на предна десцендентна артерия и циркумфлексна артерия) >70%;
- трисъдова лезия на коронарното легло в комбинация с дисфункция на лявата камера (LV) на сърцето (фракция на изтласкване на LV<50%);
- трисъдова лезия на коронарното легло с доказан голям обем на исхемичен миокард;
- двусъдова лезия със задължително засягане на проксималната предна десцендентна артерия в комбинация с ЛК дисфункция (фракция на изтласкване на ЛК<50%).
Формирането на индикации за реваскуларизация се основава на сравнение на резултатите от медицинското, ендоваскуларното и хирургичното лечение на пациенти от различни клинични групи, отразено в множество RCT, мета-анализи и големи наблюдателни регистри от последното десетилетие. Най-убедителното сравнение на PCI и CABG е извършено в рандомизираната подгрупа (n=705) на проучването SYNTAX: CABG се характеризира със значително по-висок риск от церебрални усложнения (2,7% срещу 0,3%), но значително по-ниска честота на повтарящи се реваскуларизации (6,7% срещу 12,0%, p<0,02) .
Трябва да се подчертае, че днес формулирането на показанията за използването на един или друг метод за реваскуларизация във всеки конкретен случай не се основава на догма, а се формира, като се вземе предвид анализът на ефективността и страничните ефекти на провежданата лекарствена терапия, коронарна анатомия, потвърдена исхемия и наличните резултати от сравнения на PCI и CABG в такива ситуации, оценка на техническите възможности и опит на операторите, както и избор на самия пациент. При всеки избор на реваскуларизация, лечението на пациента ще бъде комбинирано (реваскуларизация + оптимална лекарствена терапия).
Стратификация на риска
Скалите Parsonnet, Society of Thoracic Surgeons (STS), Mayo Clinic Risk Score, ACEF score, Euroscore, Euroscore II са предназначени да предскажат риска от хирургична смъртност; някои от тях включват не само възрастта и фракцията на изтласкване на LV, но и нивото на креатинина като определящи фактори. Всеки хирург преди операцията е наясно, че везните имат само консултативен характер и окончателното решение относно тактиката се взема от екипа от лекари. CABG става подходяща и показана, ако очакваната полза надвишава потенциалните опасности и животозастрашаващи рискове. Днес в ежедневната клинична практика най-използваната система е Euroscore II.
Подготовка за КШ
Предоперативният преглед на пациента включва детайлизиране на клиничната ситуация, за да се формулират индикации за CABG и стратификация на риска. Съпътстващите заболявания (захарен диабет (DM), затлъстяване, хронична обструктивна белодробна болест, патология на щитовидната жлеза) трябва да бъдат диагностицирани и максимално компенсирани на предболничния етап. Вероятно усложнение на операция с използване на машина сърце-бял дроб (ЕС) и системна хепаринизация е стомашно-чревно кървене в присъствието на неговите потенциални източници. Ние настояваме за 100% предоперативна гастроскопия дори при липса на клиника за пептична язва - за идентифициране на "тихи" ерозивни и язвени лезии; ако се открие, CABG трябва да се отложи до постигане на ендоскопска ремисия. Няма съмнение, че има повишен риск от инфекциозни следоперативни усложнения при наличие на огнища на инфекция, които не са били санирани преди операцията. Следователно търсенето и лечението на огнища на инфекция при наличие на маркери на възпаление е задължително. Санирането на устната кухина, дори без видими признаци на възпаление, е показано за всички кандидати за CABG без изключение.
При подготовката за CABG важна роля отдаваме на диагностиката и уточняването на неврологичния дефицит: както при пациенти със стенози в каротидната система, така и без такива. За оценка и ефективно намаляване на риска от неврологични усложнения, пациентите трябва да бъдат допълнително изследвани (доплероскопия на клоновете на аортната дъга, ядрено-магнитен резонанс на мозъка в ангиографски режим), ако е необходимо, консултация с невролог с цел диференциране предоперативна подготовка и подходящо лечение от първия ден на следоперативния период.
Оперативна техника
CABG операцията се извършва, за да се образува нов път на кръвния поток, заобикаляйки засегнатите области на коронарните артерии, обикновено в епикардната им част. Най-често използваните шънтове са лявата вътрешна гръдна (млечна) артерия (LIMA) и фрагменти от голямата вена сафена (GSV) на крака и бедрото. Използването на дясната вътрешна гръдна (RIMA), радиалната (LA), дясната стомашно-епиплоична артерия (RGA) и малката вена сафена се счита за алтернатива и има своите ограничения.
Най-често миокардната реваскуларизация се извършва с помощта на ЕК. Операцията започва с едновременно излагане на съдови присадки и извършване на средна стернотомия. Вените на долните крайници се изолират от отделни разрези, предимно на двата крака. LA се изолира в комбинация с придружаващи вени, като се използват мерки за предотвратяване на артериален спазъм - външно оросяване с разтвор на папаверин.
Клипсират се артериалните разклонения на ЛА.
След извършване на стандартна средна стернотомия, вътрешните млечни артерии се изолират до отваряне на перикарда, мобилизирайки крачето на присадката с околните тъкани.
След размножаване на ръбовете на гръдната кост с ретрактор, перикардът се отваря в Т-образна форма и се зашива към ръбовете на раната. След пълна хепаринизация (300-400 единици/kg тегло), аортната канюла се поставя малко по-близо до началото на брахиоцефалния ствол; за венозен дренаж по-често се използва една двулуменна канюла, прекарана през дясното предсърдно ухо в долната празна вена. Пълна ИР се извършва с умерена хипотермия до 28-32oC. Във възходящата аорта се вкарва кардиоплегична канюла. След стабилизиране на хемодинамичните параметри в изчисления режим се извършва напречно клампиране на аортата дистално от кардиоплегичната канюла и се извършва кардиоплегия чрез въвеждане на 400-500 ml студен разтвор на калий. В перикардната кухина се поставя физиологичен разтвор, замразен до консистенция на каша.
Изборът на съдове за шунтиране и приблизителната локализация на анастомозите се определя от топографията на лезията на коронарното легло. При оптично увеличение с остър скалпел епикардът се отваря над външната повърхност на артерията в зоната на анастомозата, след това луменът на артерията. Висококачественият оптичен контрол по време на тази манипулация ви позволява да изберете мястото на отваряне на артерията извън зоната на атеросклеротичната плака и да предотвратите възможно нараняване на задната стена на артерията. След това разрезът на артерията се разширява надлъжно със специализирани ножици, извити по ръба до 4-8 mm. Оформя се анастомоза на автовенозна или артериална присадка, съответстваща по размер на артериотомията. За съдов шев на автовенозно-коронарна анастомоза се използва нишка 7/0 или 8/0, за айо-артериална-коронарна анастомоза - нишка 8/0 (пролен) с атравматични игли за пробождане. Само стените на съдовете се зашиват с непрекъснат шев, околните тъкани се включват в анастомозата в случаи на изтъняване на стената на коронарната артерия и заплаха от изригване.
При тежък дифузен атеросклеротичен процес в коронарните съдове, липса на адекватен лумен за анастомоза или тежка калцификация се налага ендартеректомия. Чрез отстраняване на променената интима от коронарната артерия целият канал, както и страничните и септалните клонове се освобождават в дистална посока. След извършване на ендартеректомия се извършва шев с коронарен байпас през целия артериотомичен разрез. Дължината на такава анастомоза може да бъде повече от 3 см.
Нарастващото въвеждане на последователни („страна до страна“) анастомози, множество автоартериални CABG, използването на бимамарни Т- и Y-образни структури и IAS изискват спешно повишаване на прецизността на интервенциите и определят перспективите за използването на микрохирургични методи.
Използването на микрохирургични техники и операционен микроскоп в коронарната хирургия значително подобрява качеството на дисталните анастомози. В нашата практика използваме операционен микроскоп, монтиран на тавана или на пода. Оптичното увеличение варира в диапазона от 4-48 пъти, 6-12 пъти е достатъчно за удобна работа. Предимствата пред конвенционалните очила-лупи са:
- единно зрително поле на хирурга и асистента;
- променливо увеличение за отстраняване на технически грешки;
- добра визуализация на променената съдова стена;
- възможност за използване на микросутурен материал (нишки 8-9/0) и микрохирургични инструменти.
Трябва да се отбележи, че характеристика на тази технология е индиректното виждане на хирургичното поле за хирурга и асистента и в резултат на това необичайна ръчна координация на дисталните анастомози. Ограниченото работно поле (зрително поле 4-5 см) изисква възможност за работа с инструменти с минимални движения на ръцете.
Опитът от повече от 6500 операции на директна миокардна реваскуларизация, извършени от нас с помощта на операционен микроскоп, ни позволява да препоръчаме на сърдечните хирурзи да използват по-широко микрохирургичните техники в коронарната хирургия. Таблици 1 и 2 показват резултатите от нашето 10-годишно проследяване на пациенти, оперирани през 1998-2001 г.
За образуване на проксимални анастомози, след отстраняване на напречната скоба от аортата, се извършва странично притискане на аортата, образуват се овални перфорации, малко по-големи от диаметъра на автовенозните шънтове, ориентирани в съответствие с функционално изгодното положение на шунта. Автовенозните присадки с аорта се анастомозират с непрекъснат шев 6/0.
След миокардна реваскуларизация и стабилизиране на хемодинамиката се спира ЕК, деканулират се аортата и десните сърдечни отдели, дренират се предния медиастинум, перикардната кухина и при необходимост отворените плеврални кухини. Остеосинтезата на гръдната кост се извършва предимно с телени серклажни конци. Меките тъкани на раната се зашиват на слоеве със синтетичен конец.
Няма да е преувеличено, ако кажем, че въвеждането на коронарен байпас на млечната жлеза (MCB) през 70-те години на 20 век. бележи нова ера в коронарната хирургия, когато беше възможно значително да се подобрят както непосредствените, така и дългосрочните резултати от CABG. Революцията в хирургията, настъпила с появата на MCS, е сравнима по важност с друга, по-нова революция в интервенционалната кардиология с появата на отделящи лекарства стентове. Дългосрочната проходимост (10-15 години) на млечните шънтове надвишава 90%, което дава значително увеличение на преживяемостта. Днес използването на MCS е „златен стандарт“ в коронарната хирургия.
Бимамарното шунтиране несъмнено увеличава потенциалната полза от операцията, но не винаги може да се използва при пациенти с диабет и затлъстяване, тъй като е свързано с по-висок риск от инфекция на раната поради деваскуларизация на гръдната кост. PVHA може да се използва върху стъбло, т.е. със запазване на неговия анатомичен източник, или може да се използва като свободна артериална присадка. За съжаление все още не са налични достатъчен брой RCT, доказващи предимството на бимамарното шунтиране пред използването само на LVHA. Дългосрочните резултати от двете интервенции ще бъдат анализирани в проучването за артериална реваскуларизация в близко бъдеще.
Първоначалният опит с използването на левия ЛА като байпас показа по-лоши резултати, отколкото с венозен байпас и предизвика песимизъм. Въпреки това, с подобряването на техниките за изолиране и използването на методи за борба със спазъма, ситуацията се промени и резултатите от редица RCT потвърждават това. Много клиники са проучили възможността за използване на HSA, перспективите за рутинната му употреба все още се проучват.
Клиничната практика показва, че при млади пациенти, които не страдат от ЗД и затлъстяване, многоартериалният байпас е силно оправдан и дава надежда за добър дългосрочен резултат.
За да се минимизира загубата на кръв, се използва автотрансфузия на концентрирани измити еритроцити преди, по време и след CPB с помощта на технологията Cell Saver. Това намалява нуждата от дарена кръв, намалява честотата на кръвопреливане, белодробни, бъбречни и мозъчни усложнения, както и намалява времето за престой на пациентите в болницата с 25-30%.
KSh без IR (изключена помпа)
Интервенцията се извършва без използване на ЕК върху биещото сърце, като локалната стабилизация на миокардната област в областта на дисталната анастомоза се постига с помощта на специално разработени устройства (фиг. 1).
Първоначално тази техника е предложена като хирургична интервенция с по-нисък риск от периоперативен инсулт. В нашето проучване (то е проведено през 2007-2008 г.) това беше потвърдено. Сравнихме честотата на церебралните усложнения при CABG с CPB и без CPB сред пациенти на възраст над 70 години. В тази група, където изборът на хирургична техника без CPB е особено оправдан, инсултът се развива 3 пъти, а енцефалопатията - 2 пъти по-рядко, отколкото при "традиционния" CABG. Някои RCT обаче не показват значително намаляване на честотата на неврологични усложнения по време на CABG на биещо сърце. Предимството на тази технология все още чака своето убедително потвърждение или опровержение. Прието е, че off-pump CABG технологично не е рутинна, а комплексна интервенция и се препоръчва за извършване само във високоспециализирани центрове.
Резултати и усложнения
Смъртността в специализираните клиники е<2%. В неосложненной группе пациентов моложе 65 лет, без нарушения функции ЛЖ и клинических признаков недостаточности кровообращения 30-дневная летальность не превышает 1%. Необходимо заметить, что такой уровень летальности сохраняется уже длительное время, несмотря на то, что контингент оперированных стал значительно тяжелее и старше. Это объясняется накоплением опыта и прогрессом в анестезиологии, перфузиологии, хирургической технике, послеоперационном наблюдении и медикаментозном ведении.
Кървенето след CABG е рядко, но сериозно усложнение и се развива на фона на масивна хепаринизация поради нарушена хемостаза и функция на тромбоцитите по време на CPB. Средният обем на загуба на кръв при неусложнена CABG е 400-600 ml, което обикновено се компенсира с помощта на технологии за спестяване на кръв (Cell Saver и неговите местни аналози) и трансфузии; рестернотомия и хирургична хемостаза са необходими в 0,5-2% от случаите.
Най-честите клинично значими и прогностични ранни усложнения на CABG са церебрални нарушения, инфекция на раната и бъбречна дисфункция; периоперативен инфаркт и дълбока венозна тромбоза се развиват по-рядко.
Неблагоприятните неврологични резултати от CABG включват инсулт, делириум и така нареченото когнитивно увреждане. Въпреки напредъка на технологиите, тяхната честота, за съжаление, остава доста висока и стабилна. За илюстрация сравнихме резултатите от годишната ни дейност в различни периоди на работа - за 1995 г. и 2010 г. (Таблица 3). Сравнението само на резултатите от CABG показа, че за 15 години броят на операциите се е увеличил почти три пъти и сме успели да постигнем значително намаляване на болничната смъртност, честотата на периоперативен инфаркт, медиастинит и дори бъбречна недостатъчност. Но в борбата с церебралните усложнения успехите ни бяха много по-скромни. Най-значимите причини за мозъчните усложнения са намаляването на мозъчната перфузия и емболията, като тези причини се реализират в резултат на 3 основни точки: самият ЕК, манипулации на аортата и нарушения на сърдечния ритъм. Ние считаме комбинираното увреждане на главните артерии на главата като изключително неблагоприятен фон, на който се реализира действието на тези механизми.
Медиастинит се развива в 1-2% от случаите, рискови фактори са тежък диабет, висок индекс на телесна маса, употреба на стероиди и рестернотомия. Съвременната антибиотична терапия и използването на препарати, съдържащи имуноглобулини, често правят възможно справянето с инфекцията при така нареченото затворено лечение.
Бъбречната дисфункция, изискваща заместителна терапия, се среща при 1-5% от пациентите и може да бъде предвидена в повечето случаи; най-често срещаният му субстрат е диабетна нефропатия и хипоперфузия. Развитието на остра бъбречна недостатъчност значително влияе върху прогнозата, удължава престоя на пациента в интензивното отделение и отделението и увеличава разходите за лечение.
Най-честите следоперативни проблеми включват сърдечни аритмии (предсърдно мъждене), белодробни усложнения (плеврит, ателектаза, пневмония), постперикардиотомен синдром, анемия и нарушено зарастване на рани.
Следоперативна рехабилитация
Активирането на пациента започва на 1-вия ден от следоперативния период (полулегнало и пасивно седнало положение - на 1-вия ден, активно седнало положение в леглото, преместване на стол, преминаване във вертикално положение и ходене в отделението - от 2-ри ден). Особено внимание се обръща на ранното започване на дихателните упражнения.
За да се предотвратят ритъмни и проводни нарушения през първите 5-7 дни след операцията, е необходимо постоянно проследяване на електролитните нарушения; поддържането на нормална серумна електролитна концентрация в повечето случаи осигурява задържане на синусовия ритъм. Най-често срещаният вариант на нарушение на ритъма в следоперативния период е предсърдното мъждене.
В стандартния случай лекарствената терапия в периода на възстановяване включва:
а) основни лекарства, чиято употреба е задължителна и 100% (хепарин с ниско молекулно тегло, ацетилсалицилова киселина, антибиотик, противогъбичен антибиотик, противоязвен препарат);
б) лекарства, които не са задължителни, но много търсени в следоперативния период (β-блокери и калиеви препарати);
в) различни лекарства за симптоматично лечение (аналгетици, муко- и бронходилататори, антиаритмични средства, желязо, епоетин β).
Резултатите от изпълнението на "програмата за ускорена рехабилитация" показаха, че е възможно значително съкращаване на болничния следоперативен период - до 7-8 дни. Въпреки това, при сегашния състав на пациентите, само 15-20% от пациентите (неусложнени случаи на CABG) могат действително да влязат в тази програма; останалите изискват по-продължително възстановяване в отделението и продължаване на рехабилитацията извън отделението по хирургия. Нашият опит показва, че за успеха на оперативното лечение на днешния контингент пациенти е необходимо да се осигури период на престой в рехабилитационна институция, за предпочитане специализирана, с продължителност най-малко 14-20 дни. Целите на такова последващо лечение са: окончателно възстановяване на физическата активност и адаптиране към живота, придобиване на самочувствие и познаване на състоянието, окончателен избор на лекарствена терапия преди изписване (ако е необходимо, антикоагулантна терапия, тежък диабет). и преминаване от инсулин към перорални лекарства за последващо лечение на неврологични усложнения, анемия и др.). Още на този етап от рехабилитацията пациентът започва вторична профилактика на заболяването, която ще продължи по-нататък. В повечето западни страни тази фаза на рехабилитация се определя като времеви интервал – от 3 до 6 седмици. след изписване.
Патогенезата на промените в тялото с редовна физическа активност е изследвана, ползите от тях не се съмняват. По наше мнение и опит е необходимо да се спазват следните най-важни изисквания за планиране на физическата подготовка: редовност, дискретност, т.е. плавно стъпаловидно увеличаване на натоварването и задължително отчитане на състоянието на миокарда и наличието на аритмии при избор на модел на физическо обучение (умерено или интензивно).
Обикновено въз основа на резултатите от стрес теста се определя индивидуална програма за физическа подготовка. В проучвания за ефективността на KSh през 1980-1990 г. стана ясно, че по-голямата част от пациентите са в състояние да извършат стрес тест на 12-14-ия ден от следоперативния период и в по-голямата част от случаите със значително увеличение на двойния продукт в сравнение с предоперативния резултат. В по-голямата част от случаите критерият за прекратяване на теста с натоварване след операцията е физическата умора на пациента, по-рядко постигането на субмаксимална сърдечна честота. Резултатите от стрес теста стават отправна точка за увеличаване на обема на физическата активност и определяне на необходимостта от лекарствена подкрепа за този процес. Като адаптационен контрол се провеждат повторни тестове с физическа активност. Физическото обучение може да бъде под формата на индивидуални и групови сесии с ментор, ходене (т.е. дозирано ходене), колоездене, плуване в басейн и обучение на симулатори. Считаме, че ходенето, включително изкачването на стълби, и велоергометърът са най-приемливите видове физическа подготовка. Ние се придържаме към класическите принципи на активиране: първо увеличаваме обема на натоварването и едва след това - неговата интензивност. Когато се прилага за ходене, това означава: първо увеличете разстоянието, а след това, с уверено преодоляване на 4-5 км без почивка, темпото на ходене.
Лекарствена терапия във фазата на рехабилитация, вторична профилактика на коронарна артериална болест след CABG
Добре организираният етап на рехабилитация при пациенти след CABG става началото на вторичната профилактика на атеросклерозата. Вторичната превенция, или кардиопротективната стратегия, или фаза 3 сърдечна рехабилитация не е само програма за продължаване на физическото обучение. Това включва контрол на рисковите фактори за атеросклероза (дислипидемия, тютюнопушене, хипергликемия, артериална хипертония (АХ), затлъстяване), адекватно амбулаторно медицинско наблюдение и психосоциална подкрепа (фиг. 2).
Адекватното амбулаторно медицинско наблюдение включва назначаване на антитромботична терапия, съобразена със ситуацията и изискванията на времето; ефективна и безопасна липидопонижаваща терапия (статини, статини + езетимиб, фибрати) със задължително постигане на целеви нива на холестерол, холестерол с липопротеини с ниска плътност и триглицериди, препоръчани за високорискови пациенти; според показанията - плазмафереза, ранно откриване на стеноза и / или тромбоза на шънтове и прогресиране на коронарна атеросклероза въз основа на редовно неинвазивно изследване; своевременно решение за повторна ангиография и PCI.
Организацията на специализирана медицинска рехабилитация на пациенти с коронарна артериална болест след операции на CABG е ново направление в здравеопазването на Руската федерация. Важността на този проблем, който има не само медицинско, но и голямо социално-икономическо значение, се отбелязва в заповедта на Министерството на здравеопазването и социалното развитие на Руската федерация № 44 от 2006 г. „За последващото лечение (рехабилитация) на болни в санаториум”. В документа се говори за необходимостта от формиране на концепция за рехабилитация на тази категория пациенти в специализирани центрове за рехабилитационна медицина. За съжаление днес въпросът за взаимодействието между кардиохирургичните центрове и амбулаторните лечебни заведения остава далеч от окончателното си решение.




Литература
1. Igbal J., Serruys P.W., Taggart D.P. Оптимална реваскуларизация за сложна коронарна артериална болест // Nat Rev Cardiol. 2013. том. 10. С. 635-647.
2. Wijns W., Kolh P., Danchin N. et al. Работна група по миокардна реваскуларизация на Европейското дружество по кардиология (ESC) и Европейската асоциация по кардио-торакална хирургия (EACTS). Насоки за миокардна реваскуларизация // Eur. Heart J. 2010. Том. 31 стр. 2501-2555.
3. Shomig A., Mehilli J., de Waha A., Seyfarth M., Pache J., Kastrati A. Мета-анализ на 17 рандомизирани проучвания на стратегия, базирана на перкутанна коронарна интервенция при пациенти със стабилна коронарна артериална болест / / J Am Телефонна карта. 2008 том. 52. Р. 894-904.
4. Naik H., White AJ, Chakravarty T., Forrester J., Fontana G., Kar S., Shah P.K., Weiss R.E., Makkar R. Мета-анализ на 3773 пациенти, лекувани с перкутанна коронарна интервенция или операция за незащитени Стеноза на главната лява коронарна артерия // JACC Cardiovasc Interv. 2009 том. 2. Р. 739-747.
5. Mohr F.W., Morice M.C., Kappetein P.A. et al. Коронарен артериален байпас хирургия срещу перкутанна коронарна интервенция при пациенти с трисъдово заболяване и ляво главно коронарно заболяване: петгодишно проследяване на рандомизираното клинично изпитване SYBTAX // Lancet. Vol. 381 (2013). С. 629-638.
6. Акчурин Р.С., Ширяев А.А., Галяутдинов Д.М., Василиев В.П., Руденко Б.А., Колегаев А.С., Черкашин Д.И., Емелянов А.В., Вдовенко Ю.В. Аорто-коронарен байпас при рецидивираща ангина пекторис след ангиопластика със стентиране на коронарните артерии // Кардиологичен бюлетин. 2013. № 2. С. 12-17.
7. Nashef S.A., Roques F., Michel P., Gauducheau E., Lemeshow S., Salamon R. Европейска система за оценка на сърдечния оперативен риск (EuroSCORE) // Eur J Cardiothorac Surg. 1999 том. 16. Р. 9-13.
8. John R., Choudhri A.F., Weinberg A.D., Ting W., Rose E.A., Smith CR. Многоцентров преглед на предоперативни рискови фактори за инсулт след присаждане на коронарен артериален байпас // Annals of Thoracic Surgery. 2000 том. 69. Р. 30-35.
9. Loop F.D., Lytle B.W., Cosgrove D.M. et al. Влияние на присадката на вътрешната млечна артерия върху 10-годишната преживяемост и други сърдечни избухвания // N Engl J Med. 1986 том. 314. С. 1-6.
10. Taggart D.P., Lees B., Gray A., Altman D.G., Flather M., Channon K. Protocol for the Arterial Revascularization Trial (ART) / Рандомизирано проучване за сравняване на преживяемостта след двустранно спрямо единично вътрешно присаждане на млечна жлеза при коронарна реваскуларизация / / изпитания. 2006 том. 7. стр. 7.
11. Achouh P., Isselmou K., Boutekadjirt R. et al. Преоценка на 20-годишен опит с радиалната артерия като проводник за коронарен байпас // Eur. J. Кардиоторак. Surg. 2012. том. 41(1). С. 87-92.
12. Gottesman R.F., Sherman P.M., Grega M.A. et al. Инсулти след сърдечна хирургия: диагноза, етиология и изход // Инсулт. 2006 том. 37. Р. 2306-2311.
13. Власова Е.Е., Комлев А.Е., Василиев В.П., Ширяев А.А., Лепилин М.Г., Акчурин Р.С. Опит в ранна рехабилитация на пациенти след коронарен байпас Ангиология и съдова хирургия. 2010. № 1. С. 21-34.
14. Акчурин Р.С., Агапов А.А., Власова Е.Е., Покровски С.Н., Павлов Н.А., Творогова М.Г. Автовенозно присаждане на коронарен байпас: рискът от ранни и едногодишни оклузии на присадката при дислипидемия Торакална и сърдечно-съдова хирургия. 1996. № 2. С. 31-34.
Лекарствената терапия за коронарна болест на сърцето (ИБС) не винаги работи. Ако това се случи, тогава се взема решение за лечение на коронарна болест на сърцето чрез операция. Хирургичното лечение на ИБС е най-добрият вариант за хора в трудоспособна възраст, тъй като това лечение помага бързо да се отървете от проблема. Това означава, че човек с диагноза коронарна артериална болест ще може да възстанови работоспособността си за кратко време.
Ангиопластика - балонът притиска плаките
В какви случаи е необходима операция?
Ако причината за развитието на коронарната болест на сърцето са атеросклеротични плаки, те не могат да бъдат отстранени с лекарства, в този случай се препоръчва хирургично лечение на коронарна болест на сърцето, но това не е единствената причина. За провеждане на такава терапия трябва да бъдат изпълнени редица условия:
- Тежестта на ангина пекторис, нейното съпротивление. Ангина пекторис не се повлиява от лекарства, които са били използвани преди това. Така че трябва да има изразена клинична картина на исхемия.
- Наличие на анатомична информация относно увреждането на коронарното легло. Лекуващият лекар трябва да има данни за степента на увреждане, вида на кръвоснабдяването, броя на увредените съдове.
- Индикация за хирургично лечение може да бъде възрастта на пациента.
- Съкратителната функция на сърцето.
Забележка! Определянето на метода за лечение на заболяването се основава на последните три фактора. Те ще ви помогнат да разберете риска от операция и прогнозата за възстановяване.
Показания за хирургично лечение:
- Многобройни увреждания на коронарните артерии.
- Наличието на стеноза в стволовите артерии.
- Стесняване на устието на коронарните артерии - отдясно или отляво.
Противопоказания
При лечението на ИБС операцията не се използва в такива случаи:
- Ако са изминали по-малко от 4 месеца от инфаркт на миокарда.
- Ако миокардът е отслабен от тежка сърдечна недостатъчност.
- С намаляване на контрактилната функция на сърцето.
- В случаите, когато има множество дифузни лезии на периферните сърдечни артерии.
Методи за лечение
Има няколко начина за лечение на такова заболяване с радикален метод, сред които:
- Ангиопластика и стентиране.
- Маневрени.
- Външната контрапулсация, кардиологичната ударно-вълнова терапия са неинвазивни техники, които могат да се превърнат в алтернатива на лечението с лекарства.
Всяка техника има своите специфики и ефективност, всичко трябва да се разгледа в детайли.
Ангиопластика и стентиране
Не толкова отдавна методът беше популярен и често използван. Тази минимално инвазивна техника днес вече не е актуална. Причините са съвсем обективни - резултатът не се запазва дълго време.
Но съвременните техники позволяват да се удължи ефектът поради техниката на стентиране. Тази техника е подобна на балонната ангиопластика, но има съществена разлика - в края на балона, който се вкарва в съда на пациента, има рамка, която има тенденция да се трансформира. Изработена е от метална мрежа, която при надуване поддържа съда в разпънато състояние. И двете процедури са интервенционални, извършват се през съдове без отваряне на гръдния кош и операция на открито сърце.
 Поставяне на метален стент в съд
Поставяне на метален стент в съд Показания за операция:
- Нестабилна ангина.
- Атеросклеротично съдово заболяване.
- Инфаркт на миокарда, включително остър.
- Патология на каротидните артерии.
Ред на работа:
- На пациента се дава седатив или локална анестезия.
- През вената на бедрото до мястото на стеснението се вкарва катетър, през който се доставя контраст в целевата област, която може да се види с рентгенова снимка и стент.
- Оперирайте под рентгенов контрол.
- Когато катетърът достигне целевия съд, стентът се разширява с балон, докато достигне размера на съда. В резултат на това конструкцията се опира на стените и ги фиксира в нормално състояние.
Ефикасност и усложнения
За да се засили ефектът, има постоянно подобряване на дизайна на рамките, изработени от различни материали. Често се използват неръждаема стомана и сплави. Днес има стентове, които нямат нужда от балонно разширение – те се разширяват сами. Има стентове с функция за лечение, тъй като имат полимерна обвивка, която освобождава определена доза възстановително лекарство. Най-новата разработка са биологично разтворимите стентове, които се разтварят след 2 години.
Възможни са усложнения:
- кървене.
- Дисекция на съда.
- Бъбречни патологии.
- Хематоми на местата на пункция.
- Инфаркт на миокарда.
- тромбоза или рестеноза.
- В по-малко от 0,5% от случаите смърт.
Маневрени
Тази техника е истинско спасение, ако не могат да се използват други хирургични методи. Най-честата ситуация е, когато стенозата на сърдечната артерия е твърде тежка. Техниката е разработвана от десетилетия и много поколения лекари.
Операцията помага:
- Намаляване или намаляване на признаците на патология.
- Възстановяване на кръвообращението в сърцето.
- Подобряване качеството на живот.
Показания:
- Остра фаза на ангина, ако не се лекува с лекарства.
- Сърдечен удар.
- Остра сърдечна недостатъчност.
- Атеросклероза на артериите на сърцето.
- Стесняване на лумена с повече от 50%.
Байпасът в момента е най-радикалният метод за възстановяване на кръвообращението. По увредената артерия се създава допълнителен път за кръв. Освен това такъв път е направен не от изкуствени материали, а от собствените вени или артерии на пациента. Материалът се взема от бедрената, радиалната вена, аортата на предмишницата.
 Маневрени
Маневрени Има такива видове маневриране:
- Сърцето на пациента спира, към него е свързано изкуствено кръвообращение.
- На работещо сърце. Този метод ще ви позволи да се възстановите по-бързо и да сведете до минимум усложненията. Но за операцията е необходим голям опит на хирурга.
- Минимално инвазивна техника, която се използва при биещо и спряло сърце. В този случай е възможно да се постигне по-малка загуба на кръв и да се намалят различни усложнения, както и да се съкрати периодът на рехабилитация.
Тази техника се счита за оптимална при лечението на ИБС. При повечето пациенти се наблюдава положителен резултат от операцията. Усложненията са редки, но са възможни в тази форма:
- Дълбока венозна тромбоза.
- кървене.
- Аритмия, инфаркт.
- Нарушение на мозъчното кръвообращение.
- Инфекция на раната.
- Постоянна болка на мястото на разреза.
Какво е по-ефективно?
Невъзможно е да се отговори недвусмислено, може да се използва тази или онази техника, ако има ясни показания за това и няма противопоказания. Байпасът дава най-добър резултат с по-малко усложнения, но не е универсално решение. Лекарят избира един или друг метод въз основа на данните за здравословното състояние на пациента.
 Операцията ще ви помогне да се възстановите по-бързо
Операцията ще ви помогне да се възстановите по-бързо Заключение
Хирургичното лечение се счита за радикален метод за възстановяване на нормалното функциониране на сърцето. Два ефективни метода са се доказали от положителната страна, но те се използват само ако лечението с лекарства не работи.
Повече ▼:
Видове сърдечни операции и характеристики на рехабилитационния период след тях